پیش تر در صفحه ای مجزا در مورد دستگاه ازن مطالبی مفید را آموختیم. در این مقاله به اثرات اندازه حباب گاز ازن و pH بر رفتار ازن می پردازیم. مجموعه ای از آزمایشات بر رفتار ازن بهنگام تزریق با اندازههای مختلف حباب گاز در pH=1.7 و 7.4 انجام شد. در این آزمایشات افزایش اندازه حباب و کاهش pH سبب افزایش کارایی ازن گردید. افزایش کارایی استفاده از ازن با تغییر مسیر تولید رادیکال هیدروکسیل (OH) از تولید OH از طریق O3 به فتولیز یو وی H2O2 ایجاد شد. pH پایین باعث تغییر از طریق تعادل شیمیایی H2O2 و HO2 شد و حباب های بزرگ باعث این تغییر از طریق افزایش انتقال H2O2 از سطح حباب به محلول بودند.
معرفی تحقیق:
تولید ازن یکی از فرآیندهای اکسیداسیون پیشرفته است و برای تصفیه آب به صورت عملی استفاده شده است. اثر اکسیداسیون پیشرفته رفتار ازن بر اساس واکنش های زیر است (فتولیزO3):
- O3 + H2O + hv → O2 + H2O2
- فتولیز پراکسید هیدروژن (H2O2) H2O2 + hv → 2OH
- تولید رادیکال هیدروکسیل (OH) از طریق یون اوزونید (O3 –) H2O2 ↔ H++HO− 2
- O3 + HO− 2 → O− 3 + HO2
- HO2 ↔ H+ + O− 2
- O3 + O− 2 → O− 3 + O2
- O− 3 + H+ ↔ HO3 → O2 + OH
بر این اساس در فرآیند تولید و تصفیه توسط ازن، فتولیز H2O2 (واکنش شماره 2) و تولید OH از طریق O3 (واکنشهای 3 تا7) دو روش اصلی تولید OH را تشکیل میدهند. بسیاری از محققان تحقیقات گسترده ای را برای آشکار کردن این ویژگیها انجام دادند تا بتوانند نتایج مورد نظر را بدست آورند. برخی از این کارها عبارتند از میزان تزریق ازن، دوز UV و غیره.
با این حال، تأثیر اندازه حباب گاز ازن بر روی تصفیه ازن زیاد مورد بحث قرار نگرفته است زیرا اعتقاد بر این است که اندازه حباب گاز ازن بر انحلال ازن در آب به تنهایی از طریق تغییر در ناحیه سطحی مؤثر بین فازهای مایع و گاز تأثیر میگذارد. در این مطالعه، یک سری رفتار تحت تزریق ازن با اندازههای مختلف حباب گاز ازن در pH اسیدی و خنثی انجام شد. هدف از این مطالعه آشکار کردن اثرات اندازه حباب بر رفتار ازن در تصفیه آب بود.
در این قسمت پیشنهاد می نمائیم صفحه دستگاه تصفیه آب صنعتی ناب ملل را مطالعه فرمائید.
مواد مورد استفاده در این آزمایش:
ترکیب دی اکسان به سرعت با OH واکنش میدهد و نسبتاً با ازن غیر فعال است. بر این اساس دی اکسان به عنوان یک پروب رادیکال هیدروکسیل در این مطالعه استفاده شد. ابتدا 1.9 لیتر از محلول 2.5 میلی مولار دیوکسان برای همه آزمایش ها تهیه شد. pH در 7.4 با 0.98 میلی مولار فسفات یا توسط افزودن 1.7 اسید هیدروکلریک کنترل شد.
شکل 1 تنظیمات آزمایش را نشان میدهد. این سیستم یک بطری شیشه ای با ارتفاع 207 میلی متر و قطر 130 میلی متر بود. نور UV با یک لامپ جیوه کم فشار با طول 120 میلی متر با قدرت 20 وات تابیده شد. لامپ یووی در مرکز بطری قرار گرفته بود. دو دیفیوزر شیشه ای در زیر لامپ UV نصب شد. 40 میلی گرم در لیتر گاز اکسیژن ازن دار با تخلیه الکتریکی بی صدا از گاز اکسیژن خالص تولید شد و با سرعت جریان 500 میلی لیتر در دقیقه از طریق دیفیوزرهای شیشه ای در دسترس قرار گرفت. توجه داشته باشید که اندازه حباب گاز ازن با تغییرات در اندازه منافذ دیفیوزرهای شیشه ای کنترل میشد. شرایط آزمایشی هر اجرا در جدول 1 ارائه شده است.

روش آزمایش:
در ابتدا 1.9 لیتر محلول دی اکسان با pH تنظیم شده در سیستم افزوده شد. عمق آب 190 میلی متر بود. سپس گاز ازن از طریق دیفیوزرهای شیشه ای تزریق و لامپ یووی به طور همزمان روشن شد. محلول موجود در دستگاه به صورت دوره ای از طریق شیر نمونه برداری (برای تجزیه و تحلیل شیمیایی) نمونه برداری شد. رفتار ازن (اندازه گیری اندازه حباب و ضریب انتقال جرم) به مدت 60 دقیقه در هر بار مورد مطالعه قرار گرفت. حباب های گاز در راکتور پر شده از 1.9 لیتر محلول دیوکسان مشاهده شد. تصاویر حباب های گاز در اطراف عمق 140 میلی متر با دوربین دیجیتال پرسرعت در حالت ماکرو گرفته شده است. سپس قطر اصلی و فرعی تمامی حباب های موجود در تصاویر اندازه گیری شد. همچنین اثر شکست نور با گرفتن عکس از مقیاسی که در راکتور قرار داده شده بود تصحیح شد.
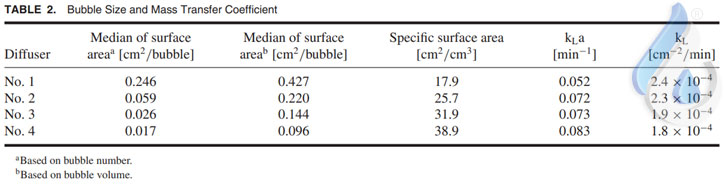
تعداد حباب های مشاهده شده برای دیفیوزر شماره یک 153 عدد، دیفیوزر شماره دو 606 عدد، دیفیوزر شماره سه 1229 عدد و دیفیوزر شماره چهار 1500 عدد بود. سطح و حجم هر حباب به صورت بیضی محاسبه شد. سطح ویژه از کل مساحت سطح حباب ها بر حجم کل حباب ها محاسبه شد. ضریب کلی انتقال جرم فاز مایع (kLa) و ثابت نرخ مصرف ازن با پیروی از Somiya و Tsuno (1975) از دادههای آزمایشهای ازنزنی منفرد برآورد شد. ضریب انتقال جرم فاز مایع (kL) از kLa تقسیم بر سطح گاز-مایع، که از سطح ویژه ضرب در نگهداشتن گاز محاسبه شد، محاسبه میشود.
تحلیل و بررسی:
دیوکسان با استفاده از یک سیستم کروماتوگرافی مایع با کارایی بالا با آشکارساز RI مورد مطالعه قرار گرفت. غلظت ازن محلول با روش نیل اندازه گیری شد. پراکسید هیدروژن با روش DMP تعیین و pH با pH متراندازه گیری شد.
نتایج
اندازه حباب و ضریب انتقال جرم:
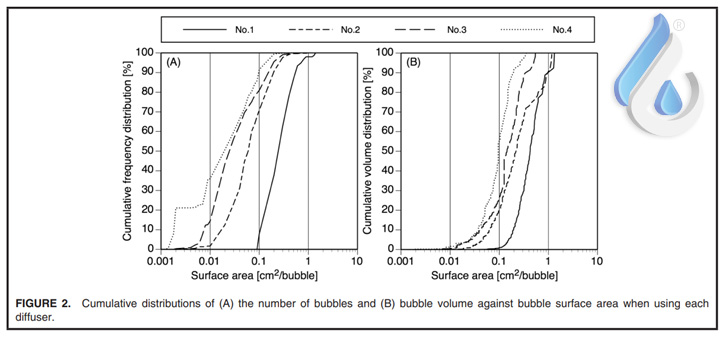
شکل 2 توزیع تجمعی حباب ها را در برابر مساحت سطح حباب نشان می دهد و جدول 2 اطلاعات اندازه حباب و پارامترهای انتقال جرم را خلاصه وار نمایش میدهد. شکل 2 و جدول 2 نشان می دهد که دیفیوزر شماره 1 بزرگترین حباب ها و دیفیوزر شماره 4 بهترین حباب های چهارگانه را ارائه میدهد. اگرچه میانه سطح حباب دیفیوزر شماره 2 کمتر از دیفیوزر شماره 1 بود، اما درصد حجمی حباب های بزرگتر از 0.6 سانتی متر مربع حباب دیفیوزر شماره 2 تقریباً برابر با دیفیوزر شماره 1 بود. در نتیجه اعداد و ارقام کیلو لیتر دیفیوزر شماره 2 مشابه با کیلو لیتر دیفیوزر شماره 1 بود. kL به طور کلی به ضخامت لایه مرزی بستگی دارد. لایه مرزی نازکتر منجر به kL بزرگتر می شود. بر این اساس، استنباط شد که ضخامت لایه مرزی اطراف حبابها در دیفیوزر شماره 1 نازکترین و در پخشکننده شماره 4 ضخیمترین ضخامت در بین چهار مورد است. از آنجایی که یک حباب بزرگ سریعتر از یک حباب کوچک جابجا میشود، تصور می شد که تغییر در ضخامت لایه مرزی ناشی از تغییر در سرعت حرکت به سمت بالا حباب ها باشد.
مقایسه رفتارهای یووی و ازن
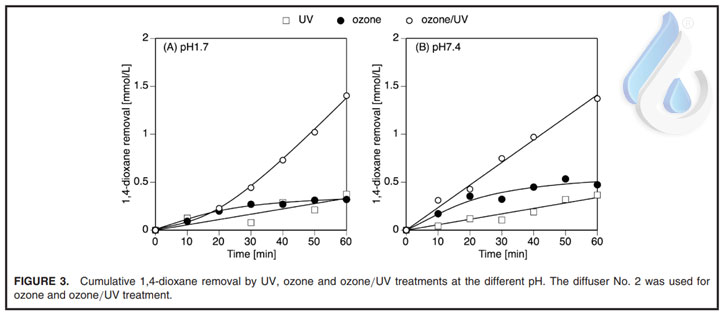
شکل 3 نمونه ای از انتقال غلظت دی اکسان را در طی آزمایشهای UV و ازن در pH 1.7 و 7.4 نشان می دهد. الگوهای انتقال با استفاده از دیفیوزرهای مختلف از نشان داده شده در شکل 3 بود. دیوکسان توسط تابش اشعه ماوراء بنفش تخریب شد و سرعت تخریب به pH محلول بستگی نداشت. دو توضیح احتمالی از تخریب دیوکسان توسط تابش UV، فوتولیز مستقیم دی اکسان و تولید OH ناشی از نور یووی بود. با این حال، فتولیز مستقیم بعید بود زیرا افرادی که آزمایش را انجام میدادند گزارش دادند که هیچ فتولیز مستقیم دیوکسان توسط تابش UV در طول موج 200 تا 400 نانومتر انتظار نمیرود. علاوه بر این، آزمایش اولیه ما نشان داد که 2.5 میلیمولار دیوکسان در 254 نانومتر از بین رفتن را نشان نمیدهد.
با توجه به دانستههای حوزه تولید دستگاه ازن میدانیم که نور خلاء یووی مستقیماً آب را به اتم هیدروژن و OH جدا می کند و این فرآیند مستقل از pH محلول است. از آنجایی که لامپ یو وی کم فشار نور خلاءUV را در 185 نانومتر تابش میکند، تصور میشد OH تولید شده از طریق فتوشیمیایی به تخریب دیوکسان کمک میکند. بر خلاف تابش اشعه ماوراء بنفش، سرعت تخریب دیوکسان توسط ازن در pH 7.4 تسریع شد. ازن OH را از طریق فرآیند خود تجزیه بیان شده توسط مدل SBH یا مدل TFGتولید می کند. انتظار می رود این فرآیند در pH بالاتر افزایش یابد. در واقع، ثابتهای نرخ مصرف ازن مشاهده شده در ازنزنی 0.030 دقیقه در pH 1.7 و 0.049 دقیقه در pH 7.4 در این مطالعه بود.
بنابراین، سرعت تخریب دیوکسان در pH 7.4 سریعتر از pH 1.7 توسط OH از طریق خود تجزیه ازن بود. فرآیند ترکیبی ازن و اشعه ماوراء بنفش سریعترین سرعت تخریب را به دلیل تولید OH نشان داد که با فتولیز یو وی ازن آغاز شد (واکنشهای 1 تا 7) بنابراین تایید شد که دستگاه ازن ژنراتور مورد استفاده به خوبی کار می کند.
مقایسه کارایی رفتارهای مبتنی بر ازن در شرایط مختلف:
برای روشن شدن تفاوتها در کارایی هر رفتار ازن حذف دیوکسان در برابر مصرف تجمعی ازن رسم شد (شکل 4). مصرف ازن تجمعی (COC [mmol-O3/L]) توسط فرمول زیر محاسبه شد
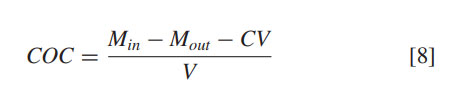
که در آن Min تزریق ازن تجمعی به سیستم [mmol-O3]، Mout تخلیه تجمعی ازن از سیستم [mmol-O3]، C غلظت ازن محلول [mmol-O3/L]، و V حجم دستگاه است [L]. شکل 4 روابط بین حذف تجمعی دی اکسان و COC را در ازن زنی و در رفتار ازن نشان میدهد.

شیب نمودارها در شکل 4 به معنای بهره وری استفاده از ازن (OUE) است که با حذف تجمعی دیوکسان در هر COC تعریف میشود. شیب ها در شکل 4 با تحلیل رگرسیون خطی 0.86±0.16 (فاصله اطمینان 95 درصد) بدست آمد. این مقدار بالاتر از OUE نظری (0.67) در تولید OH از طریق خود تجزیه ازن بود.
داده های شکل 4 شامل اثر تخریب مستقیم دیوکسان توسط مولکول های ازن است. ثابت سرعت واکنش مرتبه دوم ازن و دیوکسان را در این آزمایش 0.32 M-1 s-1 گزارش کردند. بر اساس ثابت سرعت واکنش، تجزیه مستقیم دی اکسان توسط ازن به مدت 60 دقیقه، 15±63 درصد از حذف کل دیوکسان در ازن و 1.8±1.8 درصد از کل دی اکسان بود. حذف دیوکسان در رفتار ازن شکل 4 را بوجود آورد که به شدت تحت تأثیر واکنش مستقیم ازن و دی اکسان قرار گرفت.
در نتیجه OUE در ازن زنی به حدود 1 نزدیک شد. با این حال، حذف تجمعی دیوکسان بسیار کوچکتر از رفتار ازن بود. از سوی دیگر، عملکرد ازنUV تحت تأثیر اندازه حباب و pH قرار گرفت. در شکل 4(B)، حباب های بزرگ OUE را نشان می دهند، اما جدول 1 حباب های بزرگ راندمان انحلال ازن را کمتر نشان داده است (ODE [-])، که به شرح زیر تعریف شده است:

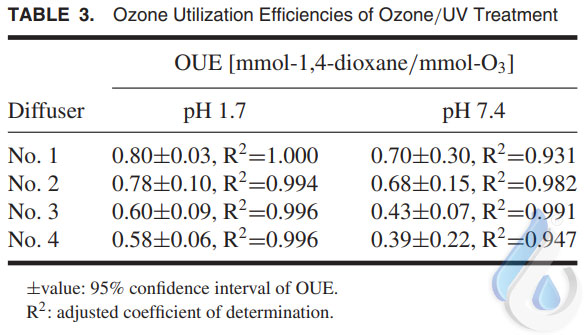
علاوه بر این، pH اسیدی تجزیه دیوکسان را در مرحله اولیه به تاخیر انداخت، اما حذف نهایی دیوکسان در pH 1.7 بیشتر از pH 7.4 بود. جدول 3 OUE در هر رفتار ازن که با شیب خط رگرسیون در محدوده افزایش خطی در شکل 4 (B) تخمین زده شده است، نمکایش میدهد. OUE مشاهده شده از 0.39 تا 0.80 متغیر بودبطوری که میزان تخریب ترت بوتیل الکل (TBA) توسط رفتار ازن را بین 0.21 تا 0.63 ازون مشاهده شد.
راندمان در این تحقیق بیشتر به دلیل تفاوت در غلظت آلاینده، 2.5 میلی مولار در این مطالعه و 1.00-1.20 میلی مولار در مطالعه آنها، و ثابت سرعت واکنش مرتبه دوم با OH بود. 6.6 × 109 M-1 s-1 برای دی اکسان و 6.0 × 108 M-1 s-1 برای TBA است. دو مسیر احتمالی تولید OH در تجزیه ازن وجود دارد، تولید OH از طریق فتولیز H2O2 (واکنشهای 1 و 2)، و تولید OH از طریق O3 (واکنشهای 1 و 3 تا 7). در هر مسیر، 1 مول ازن از نظر تئوری 2 مولOH از مسیر فوتولیز H2O2 و 2/3 مول OH از مسیرO3 تولید می کند.
با فرض اینکه یک مول OH یک مول از دی اکسان را تجزیه میکند،OUE نظری برای مسیر فتولیز 2 مول H2O2 و برای مسیر O3 میزان 0.67 مول برآورد می شود. وقتی از دیفیوزرهای شماره 1 و شماره 2 استفاده شد، OUE بالاتر از OUE نظری مسیر O3 بود. بر این اساس، مسیر فوتولیز H2O2 تا حدی به تخریب دیوکسان در هنگام استفاده از حبابهای بزرگ کمک میکند.
تأثیر pH بر رفتار ازن
همانطور که در جدول 3 نشان داده شده است، OUE در رفتار ازن در pH اسیدی افزایش یافته است. H2O2 و یون هیدروپراکسید (HO2-) در تعادل شیمیایی هستند که با واکنش نشان داده شدهاند [3]، بنابراین، اگر pH کاهش یابد، فراوانی HO2 کاهش می یابد و تولید OH از طریق O3 مهار می شود. از آنجایی که مسیر فتولیز H2O2 رادیکال OH را موثرتر از مسیر O3 تولید می کند، pH اسیدی منجر به OUE بالا می شود. با این حال، از آنجایی که ضریب خاموشی مولی H2O2 در 254 نانومتر نسبتاً کوچک است، جمع H2O2 برای تولید قابل توجه OH از طریق فتولیز H2O2 ضروری است.
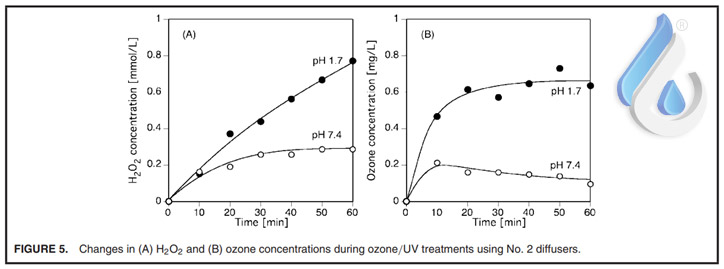
بنابراین، تصور میشود که تأخیر تجزیه دیاکسان در مرحله اولیه تحت شرایط pH اسیدی ناشی از آمادهسازی تجمع H2O2 و مهار خود تجزیه ازن باشد. شکل 5 نمونه ای از تجمع H2O2 (مجموع H2O2 و HO2-) را در طول رفتار ازن نشان می دهد و بحث فوق را تایید می کند. در pH 7.4 HO2 تولید شده توسط تفکیک H2O2 به سرعت توسط واکنش با ازن مصرف میشود (واکنش 4) علاوه بر این، خود تجزیه ازن نیز در مقایسه با pH 1.7 سریعتر انجام شد. بر این اساس، غلظت H2O2 و ازن در pH 7.4 کمتر از pH 1.7 بود. افزایش مسیر O3 و خود تجزیه ازن در pH 7.4 به تولید فوری OH و تجزیه دیوکسان بدون تاخیر زمانی کمک کرد.
تأثیر اندازه حباب گاز ازن
اندازه حباب گاز ازن تزریق شده توسط دستگاه ازن دو نتیجه داشت، کاهش ODE و افزایش OUE با افزایش اندازه حباب. اولی با تفاوت در میانگین غلظت گاز ازن خروجی در جدول 1 و در COC نهایی در شکل 4 و دومی در جدول 3 نشان داده شده است. سرعت انتقال جرم از فاز گاز به فاز مایع به kLa بستگی دارد، که حاصلضرب kL و سطح موثر (a) است. از آنجایی که نرخ جریان گاز ازن در این مطالعه روی 500 میلیلیتر در دقیقه ثابت شد، حبابهای بزرگتر منجر به ایجاد ناحیه مؤثر کوچکتر شدند. توجه کنید که ناحیه بین سطحی موثر کوچک به kLa کوچک منتهی می شود. بنابراین ODE با افزایش اندازه حباب گاز ازن بهتر نشد. افزایش در OUE با اندازه بزرگ حباب گاز ازن به فرآیند انتقال جرم H2O2 مرتبط است. از آنجایی که فتولیز یو وی ازن (واکنش1) بسیار سریع است، تصور میشود که H2O2 عمدتاً در نزدیکی سطح حباب تولید میشود. سپس H2O2 تولید شده به شکل توده در محلول پخش می شود.
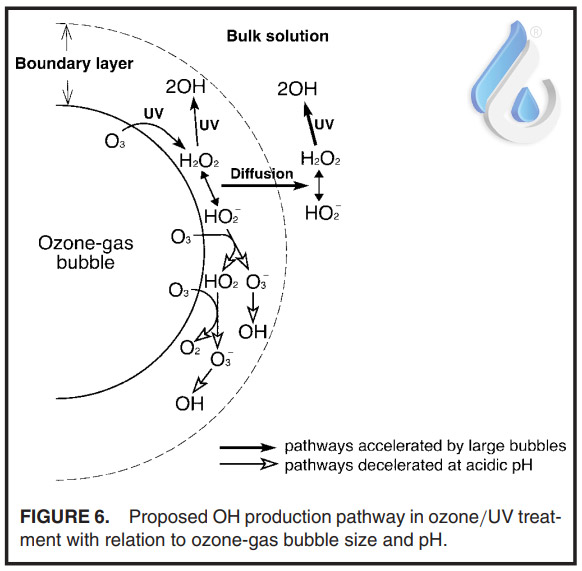
از آنجایی که سرعت حرکت به سمت بالا در حباب بزرگتر از حباب کوچکتر سریعتر است، لایه مرزی اطراف حباب بزرگتر نازکتر از اطراف حباب کوچکتر است همانطور که قبلا ذکر شد. بنابراین، زمانی که حبابهای بزرگتر گاز ازن به راکتور تزریق میشوند، فرآیند انتشار H2O2 افزایش مییابد. واکنش H2O2 در محلول حجیم به دلیل غلظت کم ازن با کمی دشواری واکنش میدهد(شکل 6)، اما در عوض توسط نور یووی فتولیز می شود. این تغییر در مسیر تولید OH از مسیر O3 به مسیر فوتولیز H2O2 منجر به افزایش OUE در هنگام استفاده از حبابهای بزرگتر شد. در pH 1.7 تفکیک H2O2 به HO2 منجر می شود. بر این اساس، O3 نیز با وجود تزریق حبابهای کوچک مهار شد. به همین دلیل است که اثر افزایش اندازه حباب بر روی OUE در pH 1.7 کمتر از pH 7.4 بود (جدول 3).
نتیجه گیری:
در این مطالعه، یک سری از رفتار ازن تحت تزریق ازن با اندازههای مختلف حباب گاز ازن در ph بین 1.7 تا 7.4 انجام شد تا اثرات اندازه حباب گاز ازن و pH بر روی رفتار ازن مشخص شود. دیوکسان به عنوان یک کاوشگر رادیکال هیدروکسیل استفاده شد. نتایج بهدستآمده به شرح زیر خلاصه میشوند:
- اگرچه تابش اشعه ماوراء بنفش و ازن به تنهایی دیوکسان را کمی تجزیه کردند، رفتار ازن سریعترین نرخ تخریب را از طریق تولید OH آغاز شده توسط فتولیز UV نشان داد.
- عملکرد رفتار ازن به اندازه حباب گاز ازن و pH بستگی دارد. افزایش اندازه حباب و کاهش pH راندمان استفاده از ازن را افزایش داد، اما کارایی انحلال ازن را بدتر کرد.
- افزایش راندمان انحلال ازن در رفتار ازن در pH بالاتر به دلیل میزان مصرف نسبتاً زیاد ازن به دلیل خود تجزیه گری و واکنش ازن و HO2 – ایجاد شد.
- اثر افزایشی pH اسیدی بر بازده استفاده از ازن با تغییر مسیر تولید OH از تولید OH از طریق O3 به فتولیز H2O2 ایجاد شد. این تغییر توسط تعادل شیمیایی H2O2 و HO2 – القا شد. فتولیز یو وی H2O2 نیاز به تجمع H2O2 در سیستم داشت، زیرا ضریب خاموشی مولی H2O2 در 254 نانومتر نسبتاً کوچک بود. این نیاز باعث تاخیر زمانی اولیه تخریب دیوکسان توسط رفتار ازن در pH 1.7 شد.
- حباب های ریز گاز ازن به بهبود کارایی انحلال ازن از طریق افزایش سطح موثر بین فازهای مایع و گاز کمک کردند.
- حباب های بزرگ ازن انتقال H2O2 از سطح حباب به محلول توده را تسریع کردند. در نتیجه، فتولیز یو وی H2O2 در محلول حجیم افزایش یافت و کارایی استفاده از ازن بهبود یافت.
از اینکه با ما تا انتهای مقاله همراه بودید از شما تشکر مینمائیم. چنانچه علاقه دارید با سایر محصولات تولیدی شرکت ناب ملل آشنا شوید می توانید روی عبارت ناب ملل کلیک نمائید.

